

Disponible en: ![]() -
- ![]() -
- ![]() -
- ![]() -
- ![]() -
- ![]() -
- ![]()
Vía de administración: vaginal
COMPOSICIÓN
Cada anillo vaginal contiene:
Etonogestrel y etinilestradiol con un promedio de 0,120 mg de etonogestrel y 0,015 mg de etinilestradiol respectivamente, cada 24 horas, durante un periodo de 3 semanas.
FORMA FARMACÉUTICA
Sistema de liberación vaginal.
FemeGyn Ring® es un anillo flexible, de polímero transparente, incoloro a casi incoloro, con un diámetro exterior de unos 54 mm y un diámetro de sección de unos 4mm.
DATOS CLÍNICOS
FemeGyn Ring® Anticoncepción.
Este medicamento está indicado para mujeres en edad fértil. La eficacia y seguridad se ha establecido en mujeres entre 18 y 40 años de edad. No se ha establecido la seguridad y eficacia de este medicamento en adolescentes menores de 18 años.
INDICACIONES
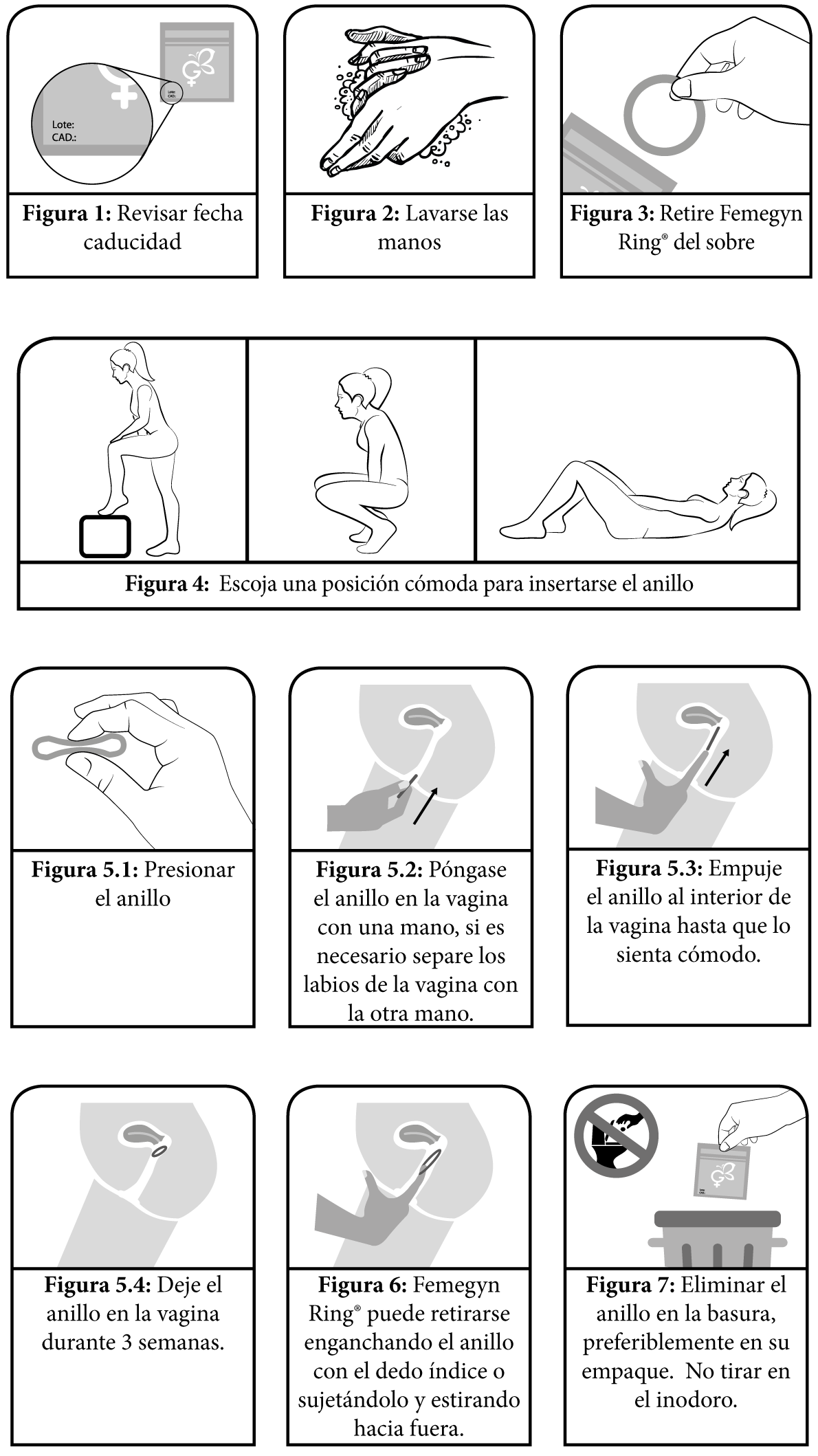
Está indicado principalmente para prevenir embarazos. El anillo vaginal funciona al impedir que el esperma llegue al óvulo. Como la mayoría de las pastillas anticonceptivas, el anillo contiene las hormonas Estrógeno y Progestina. Estas son similares a las hormonas que produce el cuerpo de manera natural. Para usar el anillo, se debe insertar dentro de la vagina y se deja dentro de la misma, para que las hormonas se absorban a través de las paredes de la vagina.
Las hormonas del anillo vaginal impiden que la ovulación ocurra. Si no hay ovulación, no habrá un óvulo que el esperma pueda fertilizar y por eso el embarazo no ocurre.
CONTRAINDICACIONES
FemeGyn Ring® está contraindicado en pacientes:
- Presencia o riesgo de tromboembolismo venoso (TEV).
- Tromboembolismo venoso: TEV actual (con anticoagulantes) o antecedentes del mismo (p. ej., trombosis venosa profunda (TVP) o embolia pulmonar (EP)).
- Predisposición hereditaria o adquirida conocida al tromboembolismo venoso, como resistencia a la PCA (incluyendo el factor V Leiden), deficiencia de antitrombina III, deficiencia de proteína C, deficiencia de proteína S.
- Cirugía mayor con inmovilización prolongada.
- Riesgo elevado de tromboembolismo venoso debido a la presencia de varios factores de riesgo.
- Presencia o riesgo de tromboembolismo arterial (TEA).
- Tromboembolismo arterial: tromboembolismo arterial actual, antecedentes del mismo (p. ej. infarto de miocardio) o afección prodrómica (p. ej. angina de pecho).
- Enfermedad cerebrovascular: ictus actual, antecedentes de ictus o afección prodrómica (p. ej. accidente isquémico transitorio, AIT).
- Predisposición hereditaria o adquirida conocida al tromboembolismo arterial, tal como hiperhomocisteinemia y anticuerpos antifosfolípidos (anticuerpos anticardiolipina, anticoagulante de lupus).
- Antecedentes de migraña con síntomas neurológicos focales.
- Riesgo elevado de tromboembolismo arterial debido a múltiples factores de riesgo o a la presencia de un factor de riesgo grave como: diabetes mellitus con síntomas vasculares, hipertensión grave dislipoproteinemia intensa.
- Pancreatitis o antecedentes de la misma si está asociada con hipertrigliceridemia grave.
- Existencia o antecedentes de hepatopatía grave, siempre que los parámetros de la función hepática no se hayan normalizado.
- Existencia o antecedentes de tumores hepáticos (benignos o malignos).
- Existencia o sospecha de neoplasias malignas en órganos genitales o mama si son dependientes de esteroides sexuales.
- Hemorragia vaginal sin diagnosticar.
- Hipersensibilidad a los principios activos o a alguno de los excipientes de este medicamento.
Femegyn Ring® está contraindicado con el uso concomitante con medicamentos que contengan ombitasvir/paritaprevir/ritonavir y dasabuvir.
PRECAUCIONES
En caso de padecer alguna enfermedad cardíaca, o insuficiencia cardíaca congestiva, hipertensión arterial, enfermedades tromboembólicas, infecciones, diabetes mellitus, indíquelo a su médico.
Es necesario aumentar la dosis de corticoides en situaciones especiales (cirugía, infecciones y otras) y por ello el médico debe conocer si el paciente sufre o ha sufrido alguna otra enfermedad.
INTERACCIONES
Se puede producir sangrado intermenstrual y/o fallo del anticonceptivo a causa de las interacciones de otros medicamentos (inductores enzimáticos) con los anticonceptivos hormonales.
Notificación de sospechas de reacciones adversas:
Es importante notificar sospechas de reacciones adversas al medicamento tras su autorización. Ello permite una supervisión continuada de la relación beneficio/riesgo del medicamento.
POSOLOGÍA
Este medicamento se administra por vía intravaginal.
El médico establecerá la dosis diaria La dosificación es individual para cada paciente, puede ser modificada por el médico en función de la respuesta al tratamiento.
SOBREDOSIS
No se han comunicado efectos adversos graves tras sobredosis de anticonceptivos hormonales. Los síntomas que pueden aparecer en este caso son náuseas y vómitos. En jóvenes puede producirse un pequeño sangrado vaginal. No existen antídotos y el tratamiento debe ser sintomático.
REACCIONES ADVERSAS
Las reacciones adversas que se han citado más frecuentemente en los ensayos clínicos con este medicamento fueron cefalea, infecciones vaginales y flujo vaginal, cada una mencionada por un 5-6% de las mujeres.
Se ha observado un aumento del riesgo de episodios trombóticos y tromboembólicos arteriales y venosos, entre ellos infarto de miocardio, accidente cerebrovascular, accidentes isquémicos transitorios, trombosis venosa y embolia pulmonar, en mujeres que utilizan AHCs.
CONSERVACIÓN
Consérvese a temperatura inferior a 30ºC al envase original.
CADUCIDAD
Este medicamento no se debe utilizar después de la fecha de caducidad indicada en el envase. (24 Meses)
VENTA BAJO RECETA MÉDICA
Los medicamentos deben mantenerse fuera del alcance de los niños.
Fabricado por:
Kern Pharma, S.A. – España
Para: Latin Farma, S.A. - Guatemala
